Analgetika Flashcards
Vad heter antagonisten (antidot) till opioider?
Naloxon
Vilka receptorer har opioider?
Delta, kappa, my
Enkephalin, dynorphin, beta-endorfin, endomorphin, nociceptin (prekursor) etc
Vad är ovan exempel på?
Endogena ligander
Vilken verkan har opioider i dorsalhornet?
- Aktionspotential från periferi i axon varpå Ca2+-kanaler (N-type) öppnas och Ca2+ flödar in varpå vesiklar frisätter neurotransmittorer i synapsklyftan
- Morfin aktiverar presynaptiska receptorer (finns även postsynaptiskt) som gör att Ca2+inflödet minskar eftersom N-type hämmas. Då frisätts mindre glutamat i synapsklyfta vilket ger mindre depolarisering av dorsalhornsneuronet och mindre nociception når hjärnan –> mindre smärta

På vilket sätt modulerar opioider top-down?
- När opioidreceptorer i PAG (mellan 3:e och 4:e ventrikel) i mecencephalon aktiveras ökar nedåtgående smärthämmande system
- Även noradrenerga system (locus coeruleus) och serotonerga system (Raphe nucleus) deltar

Utöver top-down modulering och hämning av nociception i bakhorn verkar opioider bland annat i
- Amygdala (ångest/oro)
- VTA –> Nucleus accymbens
- Thalamus
- Insula
- ACC
Var och på vilka ytterligare sätt verkar opioider?
-
Andningscentrum
- Andningsdepression som biverkan vid överdoser – antidot (naloxon iv) – toleransutveckling
- Edinger-Westphal-kärnan (n. ockulomotorius) –> mios
- Kemoreceptor trigger zone i 4:e ventrikelns golv –> illamående
- Lokala opioidreceptorer i tarmen –> förstoppning (ingen toleransutveckling)

Hur kan förstoppning vid opioidbehandling förebyggas?
- Laxantia (förebygg)
- Finns per orala opioidantagonister (naloxon) – biotillgänglighet är mkt låg (2 %), alltså ingen effekt på CNS
- Neurologisk bakgrund till opioidberoende?
-
My-receptor är viktigaste gällande beroende och de finns
- På de gabaerga interneuronen i VTA som annars håller tonisk inhibition på de dopaminerga cellerna, nu inihiberas alltså inhibitorn
- I nucleus accumbens – mer oklart hur de bidrar här
-
Morfin
- Biotillgänglighet 30 %
- Halveringstid 2-3 h
Hur metaboliseras morfin?
- Genom konjugering (M3G inaktiv, M6G aktiv)
Fentanylplåster
Vilken egenskap har fentanyl som gör att vi kan ge det som plåster?
Väldigt fettlösligt (morfin mer vattenlösligt)
-
Traditionell uppdelning mellan svaga och starka opioider
- Steg ett – NSAID, paracetamol
- Steg två – svaga opioider
- Kodein (maxdos 240 mg/dygn (motsvarar 1/10 av peroralt morfin), tramadol
- Kallas svaga då maxdos finns angiven i FASS
- Steg tre – starka opioider
Vilken typ av läkemedel är kodein och varför är det viktigt att veta?
- Prodrog då den metaboliseras till morfin via CYP2D6
- 7 % av befolkningen har mindre CYP2D6 – därför risk för utebliven effekt
- 1 % ultrasnabba metaboliserare
- Två effekter
- Låg affinitet för my-receptorn, men aktiv metabolit som har 300 ggr högre affinitet jämfört med modersubstans
- Smärtlindring via monoaminerga nedåtgående smärtinhiberande banor
- Noradrenalin, serotonin
- Benämning ”svag opioid” är traditionell och kan ge falsk säkerhet avseende beroendeproblematiken
- Maxdos 400 mg/dygn (ger ej mer smärtlindring ovan detta)
Vilket läkemedel?
Tramadol
SNRI och tricyklika på smärtindikation
- Vissa antidepressiva har analgetisk effekt
- Framför allt vid neuropatisk smärta
- Tricykliska antidepressiva bäst evidens (amitriptylin)
- Duloxetin (SNRI) – inte SSRI
Vad är verkningsmekanismen?
- Återupptagshämning av monoaminerga substanser (noradrenalin och serotonin) på spinal nivå –> förstärkning av endogen smärthämning
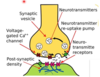
På vilket sätt kan vi smärthämma med hjälp av antiepileptika?
Neuropatisk smärta
- Ovan är första ordningens neurons axon följt av synaps och andra ordningen neuron
- Aktionspotential gör att Ca2+-kanal öppnar sig och Ca2+ inkommer och glutamat kan frisättas i synapsklyfta varpå impulsen kan gå vidare genom att AMPA aktiveras
-
Mekanism
- PREsynaptiskt – N-type kanalen kan påverkas direkt av läkemedel genom att de påverkar alfa-2-delta-subenheten vilket gör att inflöde av Ca2+ minskar och därför minskar glutamatfrisättning

Vilka viktiga antiepileptika som smärthämmar neuropatisk smärta finns det?
-
Gabapentinoider
- Gabapentin (t ex neurontin)
- Pregabalin (lyrica)
- Karbamasepein – vid trigeminusneuralgi







