Kapitel 12: Kinetik chemischer Reaktionen Flashcards
(6 cards)
Reaktion nullter Ordnung
Unabhängig von der Konzentration des Edukts (enzymatische Reaktion: pseudonullte Ordnung)

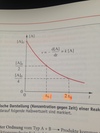
Halbwertszeit
Eine Reaktion erster Ordnung hat eine konstante Halbwertszeit. Die hälfte der ursprünglichen Moleküle reagiert in dieser Zeit.
Aktivierungsenergie
Ein Teilchen benötigt einen gewissen Mehrbetrag an Energie um reagieren zu können. Diesen Mehrbetrag nennt man Aktivierungsenergie.
Umso grösser die Aktivierungsenergie desto langsamer verläuft sie.

Kinetische Kontrolle
Die Aktivierungsenergie kann entscheidend sein, welches Produkt tatsächlich zustande kommt (auch wenn thermodynamisch ein anderes Produkt zu bevorzugen wäre, siehe Bild)

Katalysator
Ein Katalysator beschleunigt eine chemische Reaktion durch Absenkung der Aktivierungsenergie. Er beeinflusst weder die Gleichgewichtslage nocht die Gibbs-Energie ΔG0 der Reaktion. Er wird nicht verbraucht.
einstufig -> zweistufig, siehe Bild

Michaelis-Menten-Gleichung



