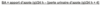Métabolisme protéines et acides aminés Flashcards
(127 cards)
Lors du métabolisme des macromolécules, que finissent par devenir les protéines, les polysaccharides et les lipides?
De l’acétyl-CoA, qui intervient ensuite dans le cycle de Krebs

Combien compte-t-on d’acides aminés différents dans la nature? Et combien sont protéinogéniques et présents chez les vertébrés?
500-600 (540 environ) dans la nature.
20 protéinogéniques et chez les vertébrés.
Quelles sont les 3 composantes de l’acide aminé?
- Acide carboxylique (-COOH)
- Fonction amine (-NH2)
- Chaine latérale variable (-R)
Qu’est ce qui est à l’origine de la différence entre les acides aminés, et quel est l’effet de cette différence?
La nature chimique de la chaine latérale, qui, par sa composition, confère des caractéristiques physico-chimiques précises.
Quelles sont les 2 formes d’un acide aminé?
Non-ionisée et ionisée

Donnez 5 exemples de caractéristiques possibles de la chaîne latérale de l’acide aminé
- Aliphatique
- Hydroxylé
- Contenant du soufre
- Diacide
- Aromatique
- Autres
V ou F? La plupart des acides aminés sont solubles dans l’eau parce que la plupart des acides aminés sont hydrophiles
Vrai
Quels acides aminés sont moins hydrophiles? Dans quoi sont-ils plus solubles?
Ceux avec une longue chaîne carbonée ( leucine, isoleucine, phénylalanine et tyrosine)
Ils sont plus solubles dans les solvants organiques (hydrophobes)
Que détermine la solubilité d’un acide aminé?
- Son pouvoir d’incorporation dans les divers tissus et organes
- La structure et la fonction des protéines
De quoi dépend la polarité des acides aminés?
De la présence d’un groupement chargé ou non sur la chaine latérale
Donnez des exemples de groupements chargés qui rendent un acide aminé polaire
-OH (hydroxyle), SH (thiol), COO-, N-
À quoi participent les groupements chargés des acides aminés polaires?
Des liaisons hydrogènes ou ioniques (ou autre)
Que confèrent les acides aminés polaires aux protéines qu’ils constituent?
- Une solubilité dans l’eau
- La formation de domaines peptidiques qui ont des fonctions biochimiques importantes, enzymatiques, immunologiques, hormonales et autre
Vrai ou faux? La chaine latérale des acides aminés non polaires participe généralement à des liaisons hydrogène ou ionique
Faux, au contraire.
Que confère l’enchainement d’acides aminés hydrophobes à la protéine? Qu’est ce que cela influence surtout?
Une hydrophobicité.
La structure 3D de la protéine
V ou F? Les acides aminés sont des acides forts et des amines forts.
Faux, ce sont des acides faibles et des amines faibles.
Quelle est la formule chimique selon laquelle se dissocient les acides aminés?
HA est la forme acide non dissociée. H+ et A- représentent les produits ionisés qui sont le proton H+ et la base conjugée A-

Qu’arrive-t-il à la réaction de dissociation plus le Ka est grand?
Plus la réaction est déplacée vers la droite et plus la forme HA est convertie vers les autres formes (H+ et A-).
Qu’est ce qui détermine la concentration du milieu?
La concentration en ion H+
Comment calcule-t-on le pKa à partir de Ka?
pKa=-logKa
Comment calcule-t-on le pH à partir de la concentration en H+?
pH=-log[H+]
C’est quoi l’équation d’Henderson-Hasselbach et qu’est ce qu’elle exprime?
pH = pKa + log [A-]/[HA]
Elle exprime la relation entre le pH du milieu et les concentrations de HA et A-
Pour un acide aminé, qu’est ce qui varie parmi les propriétés suivantes:
- le pKa
- les concentrations des différentes formes (I, II, III)
- le pH de la solution
Pour un acide aminé, le pKa est fixe mais les concentrations des formes I , II et III varient selon le pH de la solution.
L’inverse est vrai aussi , le pH de la solution variera selon les concentrations des formes I , II et III]

Combien de fonctions acide ou de fonctions amine peut contenir un acide aminé?
Un ou plusieurs acide et un ou plusieurs amine