VL 4: Stoffwechsel II Flashcards
(40 cards)
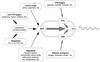
Entner-Douderoff-Weg (KDPG-Weg) Reaktionsschritte
- Glucose-6-P wird zu 6-Phosphogluconat dehydrogeniert
- Bildung von KDPG durch Abspaltung von H2O (=2-Keto-3-desoxy-6-phosphogluconat = charakterisisches Zwischenprodukt)
- KDPG wird durch Aldolase zu Pyruvat und GAP gespalten

KDPG-Weg
- Ausschließlich bei Bakterien (modifiziert bei Archaen)
- Transport von Glucose über ein H+ Symportsystem (PEP kann für Anabolismus verwendet werden)
- erhebliche Anzahl von Bakterien besitzt nicht die vollständige Ausstattung der Enzyle für den klassischen EMP-Weg der Glykolyse
- nur 1 ATP vs. 2 ATP bei EMO
- Bilanz
- 2 Pyruvat
- 1 ATO
- 2 NADH + H+
Pentosephosphat-Weg zur vollständigen Oxidation von Glucose
Reaktionsschritte
- Glucose-kinase-Reaktion
- als erster Schritt
- wie inder Glykolyse
- Umwandlung Hexose in Pentose
- wird als Bustein für Biosynthese von Nukleinsäuren und Co-Enzymen benötigt
- Bildung von 2 NADPH
- Oxidation von Glu-6-P durch 2 Dehydrogenierungsschritte zu Ribulose-5-P
- Zyklischer Prozess
- 3-Pentose-Phosphat werden in 2 Fluctose-6-P und ein GAP umgewandelt
- Durch Isomerisierung von F6P zu G6P und Kondensation von 2 Triosephosphaten zu einem Hexosephosphat schließt sich der oxidatidative Pentosephosphatweg
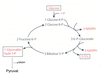
Pentose-Phosphat-Weg
- Bilanz
- 1 Pyruvat
- 1 ATP
- 6 NADPH
- 1 NADH
- 3 CO2
- Nebenweg für die Bereitstellung von wichtigen Ausgangssubstanzen (Pentosephosphate, GAP und Reduktionsäquivalente (NADPH) für Syntheseprozesse
- in Bakterien mit unvollständigen Citratzyklus auch zur vollständigen Oxidation von Glucose zu CO2 (d.h. Energiegewinnung)
- Umwandlung der Zucker ineinander ist reversibel
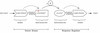
Wichtigste Glucose-Abbauwege bei Prokaryoten
*

Pyruvat als zentrale Schlüsselverbindung des Energiestoffwechsels

Aerober Stoffwechsel
- sökjf
Bildung von Acetyl-CoA
- oxidative Decarboxylierung
- Pyruvat wird zu Acetyl-CoEnzym A oxidiert
- irreversibel
- Acetyl-CoA ist ein aktivierter Essigsäurerest

Tricarbonsäure (Zitrat) Zyklus
- Gewinnung von Energie (GTP) und Reduktionsmittel (NADH, FADH2) durch Abbau von Acetyl-CoA im Citratzyklus
- bei diesen Vorgängen wird der Acetylrestdes Acetyl-CoA schrittweise zu CO2 und Wasser abgebaut
- Die im Citratzyklus gewonnenen Coenzyme (NAD+ und FAD) gebundenen Elektronen werden der Atmungskette zugeführt und auf den terminalen E-Akzeptor O2 übertragen
- Die dabei frei-werdende Energie wird genutzt um ATP zu bilden
- Der Zitratzyklus dient außerdem als Lieferant verschiedener Vorläufermoleküle für den Anabolismus
- Bspw. können alpha-Ketosäuren in dem Zyklus entnommen werden, um daraus AS oder andere Stoffe zu bilden

Zitratzyklus - Reaktionsschritte

Bilanz der Glucose-Oxidation zu O2
- der überwiegende Anteil der freien Energie der Glucose-Oxidation (deltaG0’ = -2870 kJ/mol) befindet sich noch in den Reduktionsäquivalenten
- Die Regenerierung der Coenzyme NAD+ und FAD durch Reoxidation der Reduktionsäquivalente NADH und FADH2 in Elektronentransportketten ist mit Energiegewinn verbunden

Chemiosmotische Kopplung
- ATP wird hauptsächlich durch die Oxidation von NADH regeneriert
- elektrochemisches Potential an der Mitochondrien-Membran (über diee Cytoplasmamembran von Bakterien)
- außen höhere Konzentration von H+ Ionen als innen = Protonengradient
- NADH-Oxidation in einer ETK = nach außen gerichtete Protonenpumpe
- Protonentranslokation produziert eine Proton Motive Force deltaP (PMF)
- Elektronenransportphosphorylierung = ETK liefert die Energie für die Phosphorylierung von ADP zu ATP

Atmungskette
- Spezialfall einer ETK = aus einer Reihe hintereinander geschalteter Redox-Moleküle, die in der Lage sind, Elektronen aufzunehmen bzw. abzugeben
- Über diese Kette werden Elektronen von höheren Energieniveaus auf niedrigere weitergegeben

Komplexe der Atmungskette
- Komplex I
- NADH: Ubichinon-Oxidoreduktase oder NADH-Dehydrogenase
- reduziert Ubichinon mittels NADH, vor allem aus dem Citratzyklus
- Komplex II
- Succinat: Ubichinon-Oxidoreduktase oder Succinat-DH (aus dem CZ)
- Succinat wird zu Fumarat oxidiert und Reduktion von Ubichinon
- Komplex III
- Ubihydrochinon (Ubichinol): Cytochrom c-Oxidoreduktase oder Cytochrom-c-Reduktase
- Komplex IV
- Cytochrom c: O2-Oxidoreduktase oder Cytochrom-c-Oxidase
- Cytochrom c wird oxidiert und Sauerstoff zu Wasser reduziert

Vergleich bakterieller und mitochondrieller ETK
oxidase-positive vs. Oxidase-negative Bakterien
- viele Bakterien haben kein Cytochrom c
- oxidieren das reduzierte Ubichnol direkt mit Hilfe anderer Andoxidasen (Chinol-Oxidasen)
- ähnelt Cytochrom c-Oxidase und enthalten im aktiven Zentrum eine Häm-Gruppe und ein Kupfer-Ion

ATP Synthase F1F0
Rotor nutzt Protonengradient
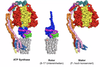
ATP Synthese/Hydrolyse (F1)
3 Schritte
- 3 ATP Hydrolyse für 1 Rotation
- ab-UE 3 verschiedene Konformationen
- loose, tight, open
- gamma-UE bewirkt Konformationsänderung

ATP-Synthese im F1(alphabeta)3-Komplex
Die Drehung des Rotors um 360° liefert in drei Schritten drei Moleküle ATP

Rotation durch pmf (F0)
Protonierung des Asp61 der c-UE
- 10 c-UE im E.coli F0-Rotor
- im Ruhezustand sind alle Asp61 (mit Ausnahme eines Asp61) proponiert
- poositiv-geladener Arg-Rest der a-UE wird durch ionische WW neutralisiert
- Proton wird ins Cytoplasma entlassen
- deprotonierter Asp 61 des gegenüberliegenden cPeptids führt zur Konformationsänderung
- Rotation des c-Rings um 36°
- unterschiedliche Anzahl an F0-c Peptide

ATP-Ausbeute bei E. coli

Protonenmotorische Kraft

Konsequenzen des Lebens in Gegenwart von Sauerstoff
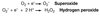
Schutzmechanismen vor toxische Sauerstoffbindungen

Anaerober Stoffwechsel
Respiration ohne Sauerstoff